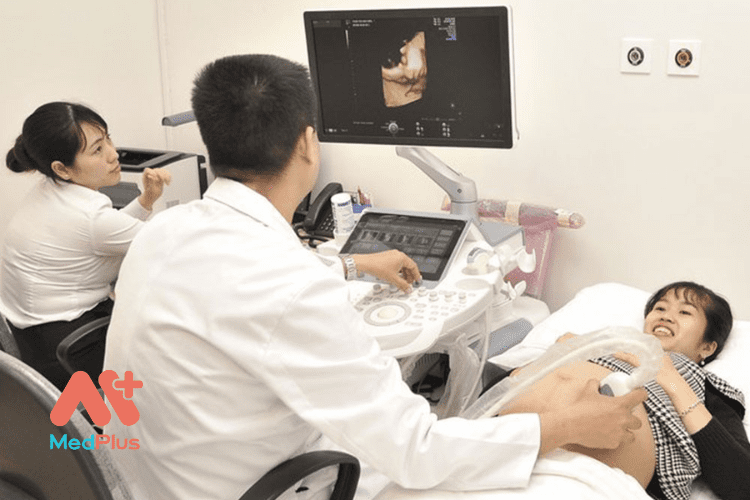
Các bệnh tự miễn hợp thành một nhóm bệnh không đồng nhất. Chúng thường được điều trị bằng thuốc chống viêm, ức chế và điều hòa miễn dịch. Kết quả nhận được trong hầu hết các trường hợp rất khả quan. Tuy nhiên, một số bệnh nhân bị kháng các liệu pháp thông thường. Việc sử dụng thuốc liều cao trong những trường hợp gây hại tủy xương. Tình huống này đã kích thích việc nghiên cứu tế bào gốc tạo máu để điều trị bệnh tự miễn. Bài Cách trị bệnh tự miễn: Liệu pháp tế bào và giá trị ứng dụng trình bày chi tiết vấn đề.
Cách trị bệnh tự miễn: Liệu pháp tế bào và giá trị ứng dụng
1. Giới thiệu
Khái quát
Các bệnh tự miễn dịch (AD) xuất hiện do
- mất cân bằng miễn dịch và giảm khả năng chống chịu,
- khiến hệ miễn dịch tấn công các mô bên trong cơ thể,
- các phức hợp miễn dịch khiến kháng thể tự lưu hành và tế bào lympho T tự hoạt động.
Vấn đề
Cách trị bệnh tự miễn thông thường có hiệu quả ở hầu hết bệnh nhân. Nhưng một số bệnh nhân kháng lại các tác nhân chống viêm và ức chế miễn dịch. Và họ chuyển sang dùng thuốc liều cao. Trong những trường hợp này, họ cần phải phục hồi tủy xương (BM). Vì vậy cách trị bệnh miễn dịch trong trường hợp này diễn ra theo quy trình
- thuốc ức chế miễn dịch liều mạnh,
- cấy ghép tế bào gốc tạo máu (HSCT).
Nhóm bệnh miễn dịch
Phương pháp điều trị thay thế này hỗ trợ các bệnh nhân mắc các bệnh miễn dịch. Chúng bao gồm
- đa xơ cứng (MS),
- xơ cứng toàn thân (SS),
- viêm khớp dạng thấp (RA),
- viêm khớp vô căn vị thành niên (JIA),
Hiện trạng
Ý tưởng
HSCT được xem như một cách trị bệnh tự miễn. Và nó đã được nghiên cứu từ những năm 1970. Sự thành công của phương pháp này
- đã được chứng minh rộng rãi trên các mô hình động vật,
- và những bệnh nhân cấy ghép BM mắc AD.
Ví dụ, cấy ghép BM toàn thân (BMT) dự kiến chữa các bệnh thiếu máu bất sản ở 2 bệnh nhân bị RA. Đồng thời nó đã làm thuyên giảm hoàn toàn RA trong ít nhất 11 năm (2).
Thực nghiệm
Bước 1
Cách trị bệnh tự miễn bằng tế bào gốc ngày càng phổ biến. Đến năm 2004, ngân hàng dữ liệu châu Âu và Bắc Mỹ đã tích lũy thông tin về khoảng 800 bệnh nhân được tuân thủ HSCT để trị nhiều loại bệnh (3). Hầu hết các thủ tục này liên quan đến liệu pháp HSCT tự thân máu ngoại vi (AHSCT). Sau khi kích thích cơ thể bệnh nhân huy động các tế bào gốc từ BM đến máu ngoại vi,
- máu của bệnh nhân được thu thập và xử lý,
- và các tế bào trưởng thành bị loại trừ cho đến khi thu được đủ số lượng HSC để cấy ghép.
Bước 2
Sau đó, bệnh nhân được
- xạ trị / hoặc gây độc tế bào,
- loại bỏ các tế bào đang phân chia, bao gồm cả các tế bào miễn dịch.
Nhận định
Máu đã qua xử lý được trả lại cho bệnh nhân thông qua truyền máu. Và nó diễn ra theo một cơ chế di chuyển. Các HSC di chuyển đến BM, nơi chúng bắt đầu quá trình biệt hóa thành các tế bào chức năng trưởng thành. Phương pháp điều trị này đã được chứng minh
- giúp tái lập khả năng chịu đựng,
- và giảm sự tái phát của AD.
2. Tế bào gốc
Tế bào gốc được đánh giá cao bởi khả năng
- tự đổi mới,
- biệt hóa đa tuyến,
- tăng sinh,
- huy động,
- và hoạt động (4).
Tế bào gốc có thể được chia thành hai nhóm chính:
- tế bào gốc phôi (ESCs),
- và tế bào gốc trưởng thành (ASCs).
Đặc trưng
ESCs
Chúng được tìm thấy trong phôi cho đến khoảng 3 ngày sau thụ tinh. Chúng có khả năng tạo ra hơn 200 loại tế bào, bao gồm cả các mô ngoài phôi như nhau thai và dây rốn. ESCs
- thu được bên trong tế bào hình thành phôi nang,
- vào thời điểm 4 hoặc 5 ngày sau khi phôi được thụ tinh.
Nhưng trước khi làm tổ trong tử cung, chúng vẫn là các tế bào đa năng (5). Nghĩa là, chúng có khả năng tạo ra tất cả các loại tế bào, ngoại trừ các mô ngoài phôi.
ASC
Chúng làm phát sinh các tế bào tiền thân của mô cụ thể. Và trong hầu hết các trường hợp, chúng là tế bào đa năng. Nhưng chúng chỉ tạo ra một số loại tế bào. Tế bào gốc
- được sử dụng phổ biến nhất trong y học lâm sàng là HSC,
- một loại ASC đa năng, tạo ra tất cả các loại tế bào máu và hệ thống miễn dịch (5).
Các nguồn chính của HSC là
- BM,
- máu dây rốn (UCB),
- và máu ngoại vi với số lượng nhỏ hơn.
Đặc biệt
Một số loại ASC dường như có khả năng biệt hóa. Quá trình này được xác định nhờ việc biệt hóa một tế bào tiền thân thành một dòng tế bào khác nguồn. Một ví dụ tế bào gốc BM được kích thích để tạo ra tế bào thần kinh (6). Sau đó, tế bào gốc đa năng, chẳng hạn như
- tế bào gốc trung mô (MSC),
- và tế bào tiền thân trưởng thành đa năng,
được phát hiện trong một số mô trưởng thành.
Trong các phần tiếp theo, chúng tôi báo cáo một số cách trị bệnh tự miễn bằng liệu pháp tế bào. Ngoài ra, chúng tôi trình bày
- các quy trình điều trị khác nhau được sử dụng,
- và thảo luận về những hạn chế, ưu điểm của các quy trình đó.
3. Một số cách trị bệnh tự miễn cụ thể
3.1. Viêm khớp dạng thấp và viêm khớp vô căn ở trẻ vị thành niên
Ý tưởng
Cấy ghép tế bào gốc tự thân (ASCT) đã được đề xuất như một phương pháp điều trị khả thi cho các bệnh AD nặng như
- RA,
- MS,
- SS,
- và SLE.
Gần 1000 bệnh nhân mắc các chứng rối loạn tự miễn khác nhau đã trải qua liệu pháp ASCT kể từ năm 1996. Trong số đó có một số ít trẻ em, phần lớn bị JIA (7).
Đặc trưng
RA là một bệnh AD toàn thân, về lâu dài, nó có thể khiến bệnh nhân
- bị mất khớp,
- mất khả năng vận động,
- giảm cả chất lượng cuộc sống và tuổi thọ.
Các đáp ứng miễn dịch tế bào và dịch thể có thể góp phần vào việc chữa các tổn thương. Các tế bào dạng thấp, một kháng thể đặc hiệu cho vùng Fc của IgG ở người. Chúng được tìm thấy ở 80% bệnh nhân bị RA (8).
Các tế bào liên quan đến phản ứng viêm có nguồn gốc từ HSC. Điều này cho thấy bệnh này có thể bắt nguồn từ các vấn đề ở tế bào gốc. Không rõ liệu
- các tế bào viêm có nguồn gốc từ các tế bào gốc bất thường,
- hay chúng là các tế bào tiền thân bình thường
- có khả năng gây bệnh trong một môi trường vi mô chủ yếu bị chiếm giữ bởi các cytokine gây viêm.
Bằng chứng cho thấy khiếm khuyết nằm trong tế bào gốc là thực tế. RA có thể được truyền hoặc loại bỏ bằng cách cấy ghép tế bào gốc đa năng (9).
Thực nghiệm
Một giả thuyết liên quan đến RA là nó liên quan đến sự lão hóa của tế bào gốc. Loại haplotype HLA-DR4 dường như được liên kết với RA. Những người có HLA-DR4 + khỏe mạnh có biểu hiện lão hóa sớm HSC.
Tế bào T già biểu hiện các thụ thể điều hòa miễn dịch riêng biệt giúp tăng cường hoạt động của chúng, độc lập với sự nhận biết kháng nguyên. Các tế bào này có đặc tính chống viêm và kích hoạt phản ứng tự động.
Trong RA, hoạt động bất thường của tế bào gốc có thể không chỉ giới hạn ở HSC, mà còn có thể liên quan đến MSC. Do đó, sự lão hóa sớm của tế bào gốc trong RA có thể dẫn đến
- sự phá hủy mô do hoạt động của tế bào T,
- và làm thất bại cơ chế dung nạp (10).
Lược sử
Nghiên cứu ứng dụng tế bào gốc trong điều trị RA bắt đầu từ đầu những năm 1980 trên mô hình động vật. Các nghiên cứu lâm sàng chủ yếu liên quan đến các HSC tự thân hoặc hiếm hơn là BMT đồng sinh hoặc đa năng (11). Quy trình cấy ghép khác nhau giữa các nghiên cứu.
Giống như trong các AD khác, để thực hiện liệu pháp AHSCT máu ngoại vi, các tế bào được huy động bằng cách
- sử dụng yếu tố kích thích tế bào hạt (G-CSF) có hoặc không có ức chế miễn dịch, trước khi di chuyển bạch cầu.
- việc cấy ghép có thể có hoặc không có thao tác in vivo hoặc ex vivo bằng cách sử dụng globulin kháng tế bào máu (ATG) và / hoặc bằng cách lựa chọn CD34 +ô, điểm đánh dấu HSC.
Xu hướng
Mục đích của các quy trình này là loại bỏ các tế bào lympho hoạt tính tự động trưởng thành. Do đó ngăn chúng tái nhập vào cơ thể. Một quá trình ức chế miễn dịch diễn ra ở cường độ cao. Tiếp đó các tế bào gốc được tái sản xuất trong thụ thể.
Một số nghiên cứu lâm sàng được thảo luận trong suốt nghiên cứu tổng quan này. Các bệnh nhân được chọn trong các nghiên cứu sau đây
- có biểu hiện RA nặng,
- đã được chứng minh là có khả năng kháng lại các liệu pháp thông thường.
Huy động HSC và G-CSF được coi là một kỹ thuật phù hợp
Tuy nhiên, việc sử dụng cyclophosphamide (CY) trước G-CSF dường như mang lại một số lợi ích. Sự ức chế miễn dịch do CY gây ra có thể làm giảm nguy cơ tăng cường các triệu chứng RA do G-CSF tạo ra. CY dường như
- làm tăng mức HSC,
- tạo điều kiện thuận lợi cho thao tác ghép,
- và giảm số lượng tế bào lympho T gây bệnh có khả năng khiến bệnh tái phát.
Hơn nữa, nó dường như
- kích thích sự đổi mới của các tế bào có đủ năng lực miễn dịch,
- thiết lập lại sự cân bằng miễn dịch, mà không cần truyền lại HSC (12).
Đánh giá
Chế độ điều hòa này mang lại hiệu quả tuyệt bởi giảm độc tính. Do đó, liều CY được sử dụng đã được thiết lập là 200 mg / kg. Vì nó tạo ra phản ứng hiệu quả trong điều trị RA và thể hiện mức độ độc tính chấp nhận được (13). Trong một nghiên cứu liên quan đến 4 bệnh nhân nhận CY và ATG,
- 1 bệnh nhân được chiếu xạ toàn thân (TBI),
- 2 bệnh nhân, bao gồm cả bệnh nhân đã nhận TBI, có biểu hiện tái phát bệnh sau cấy ghép,
- mặc dù các triệu chứng nhẹ và thoáng qua.
- 2 bệnh nhân còn lại đạt mức cải thiện ACR70.
Theo American College of Rheumatology (ACR), ACR70 tương ứng với mức cải thiện 70% về mức độ
- đau khớp và phù nề,
- cải thiện 70% ở ít nhất 3 trong số 5 thông số, bao gồm cả mức độ phản ứng Protein C, lắng hồng cầu, và mất khả năng hoạt động.
Tương tự, ACR20 và ACR50 tương ứng với mức cải thiện lần lượt là 20 và 50% (14).
Sự thật
Nghiên cứu về việc sử dụng CY liều cao trong trường hợp không tái truyền tế bào gốc dựa trên nồng độ cao của aldehyde dehydrogenase, một loại enzyme chịu trách nhiệm đề kháng tế bào của CY (9). Và 2 bệnh nhân đã cho thấy bệnh thuyên giảm hoàn toàn (15).
Moore và cộng sự (16) đã nghiên cứu 33 bệnh nhân ngẫu nhiên để cấy ghép tự thân của các tế bào không thao tác hoặc cấy ghép các tế bào CD34 + đã chọn.
Hiệu quả của việc sử dụng tế bào gốc không thao tác tốt hơn những tế bào CD34 + được chọn lọc. Trong một ca cấy ghép đồng bộ HSC,
- bệnh nhân RA nhận HSC từ người anh em song sinh của mình,
- không thấy bệnh tái phát trong ít nhất 24 tháng.
Đặc biệt
Có một số khác biệt trong biểu hiện của một số kiểu thụ thể tế bào T phụ giữa hai anh em. Sau khi cấy ghép, bộ phận tiếp nhận tế bào T của vật chủ trở nên giống bộ phận hiến tặng. Do đó, các tế bào lympho tổng hợp từ một người hiến tặng khỏe mạnh có khả năng
- sửa đổi chứng rối loạn điều hòa miễn dịch,
- góp phần tạo ra tình trạng miễn dịch ghép so với tự miễn dịch (17).
Hầu hết các nghiên cứu về HSCT liên quan đến các trường hợp cá biệt hoặc các nhóm mẫu nhỏ
Một nghiên cứu rộng hơn, dựa trên hồ sơ của cả Châu Âu về Cấy ghép Máu và Tủy (EBMT) và Cơ quan Đăng ký Cấy ghép Tủy và Máu tự thân,
- liên quan đến việc thu thập kết quả từ khắp nơi trên thế giới về các trường hợp điều trị RA bằng tế bào gốc,
- đặc biệt trường hợp nặng và kháng thuốc.
Điểm lược
Từ năm 1996 đến năm 2000, 76 bệnh nhân đã được đăng ký. Tỷ lệ tử vong liên quan điều trị thấp, với 1 bệnh nhân tử vong, người đã được thanh lọc mảnh ghép và ức chế miễn dịch. Hầu hết bệnh nhân đều đáp ứng tốt điều trị, mặc dù tỷ lệ tái phát cao. AHSCT giúp kiểm soát bệnh bằng việc sử dụng các loại thuốc chống đau bụng thông thường.
Do đó, HSCT trong liệu pháp RA được bệnh nhân dung nạp tốt, ít trường hợp tử vong liên quan đến cấy ghép. Hiện tại, AHSCT không được coi là một liệu pháp điều trị RA. Tuy nhiên, nó có thể đại diện cho một khả năng có thể “trở lại thời kỳ đầu của cơ chế bệnh”, tạo điều kiện thuận lợi cho việc kiểm soát sự gia tăng triệu chứng thông qua việc sử dụng liệu pháp duy trì (9).
Việc duy trì sau cấy ghép này là trọng tâm của EBMT / EULAR (Liên minh Châu Âu chống bệnh thấp khớp) Cấy ghép tế bào gốc tự thân vào thử nghiệm quốc tế về bệnh viêm khớp dạng thấp (3). Tuy nhiên, thử nghiệm này đã bị đình chỉ vì không đủ bệnh nhân.
Vấn đề
JIA toàn thân là một dạng viêm khớp không đồng nhất và chiếm 10 – 20% tổng số các trường hợp JIA ở người da trắng ở Bắc Mỹ và Châu Âu. Có tới 30% bệnh nhân vẫn còn bệnh sau 10 năm và tỷ lệ mắc bệnh trong nhóm này cao (18). Bất chấp các liệu pháp hiện đại, JIA vẫn là một nguyên nhân quan trọng gây ra bệnh tật ở trẻ em. Vì nó thường không đáp ứng với các chất chống TNF.
Kể từ năm 1997, HSCT đã được áp dụng như một quy trình thử nghiệm cho hơn 50 trẻ em mắc bệnh JIA. Trong một phân tích hồi cứu dữ liệu theo dõi trên 34 trẻ em bị JIA được điều trị bằng ASCT tại 9 trung tâm cấy ghép khác nhau ở châu Âu,
- kết quả cho thấy 18 trong số 34 bệnh nhân (53%)
- đã thuyên giảm hoàn toàn không cần dùng thuốc vào thời điểm theo dõi từ 12 đến 60 tháng.
Trong số 7 bệnh nhân này, việc điều trị bằng kháng TNF đã thất bại
Sáu trong số 34 bệnh nhân (18%) cho thấy đáp ứng một phần (cải thiện từ 30 đến 70%) và 7 (21%) đề kháng với ASCT. Có 3 trường hợp tử vong liên quan đến cấy ghép (9%) và 2 trường hợp tử vong liên quan đến bệnh tật (6%).
Những kết quả này cho thấy rằng ASCT ở những bệnh nhân bị bệnh JIA nặng
- giúp thuyên giảm bệnh,
- không cần dùng thuốc,
- và làm tăng đáng kể sức khỏe chung đáng kể,
- nhưng thủ thuật này có nguy cơ tử vong cao (19).
Hứa hẹn
Gần đây hơn, nguy cơ này đã được giảm bớt bằng cách điều trị trước bằng steroid cho những bệnh nhân mắc bệnh rất nặng trước khi cấy ghép. Nhóm Cấy ghép tủy xương châu Âu có kế hoạch tiếp tục sử dụng ASCT trong điều trị JIA,
- đặc biệt là dạng khởi phát toàn thân của bệnh,
- với fludarabine trong phác đồ điều trị và có thể,
- trong tương lai, MSC được dùng thay vì HSC.
Chỉ có 1 bệnh nhân bị RA được cấy ghép trong Thử nghiệm Hợp tác Brazil về Cấy ghép Tế bào gốc Tạo máu Tự thân. Một bệnh nhân nữ 20 tuổi mắc dạng đa bào JIA được điều trị bằng
- chế độ điều hòa CY (200 mg / kg),
- và ATG (4,5 mg / kg),
- và tế bào gốc máu ngoại vi tự thân vào tháng 9/2005 tại Bệnh viện Sírio Libanês ở São Paulo.
Kháng thể đơn dòng chống CD20 (Rituximab) đã được đưa ra (375 mg / m2 3 tháng một lần) để
- ngăn ngừa tái phát,
- và bệnh nhân duy trì tình trạng thuyên giảm hoàn toàn sau 1 năm theo dõi.
3.2. Lupus ban đỏ hệ thống
Đặc trưng
Có bằng chứng cho thấy bệnh nhân SLE, một bệnh AD toàn thân,
- có biểu hiện rối loạn chức năng BM,
- với số lượng tế bào CD34 + giảm rõ rệt,
- và có thể giảm khả năng tăng sinh tế bào gốc.
Các bệnh nhân
- có mức độ apoptosis tăng cao trong tiểu quần thể tế bào CD34 +
- và giảm tần suất các đơn vị hình thành khuẩn lạc.
Những bất thường này dường như
- liên quan đến một khiếm khuyết trong môi trường vi mô của BM,
- mâu thuẫn với giả thuyết rằng chúng có liên quan đến một số khiếm khuyết chính trong tế bào gốc.
Quan sát
Trong giai đoạn sau khi cấy ghép, số lượng tế bào CD34 + tự chết giảm đi đáng kể (21).
EBMT và EULAR đã công bố 53 trường hợp bệnh SLE sử dụng HSCT từ năm 1995 đến 2002. Tại Hoa Kỳ, một trung tâm cấy ghép đã báo cáo việc sử dụng HSCT trong 50 trường hợp từ năm 1997 đến 2005 (21). Hiện tại, các đề cương nghiên cứu sử dụng một phác đồ điều hòa bao gồm
- huy động CY và G-CSF,
- liều cao CY và ATG,
- và chọn lọc tế bào CD34 + in vitro (21,22).
Kết quả
Bên cạnh các bệnh nhân SLE được báo cáo trong các nghiên cứu EBMT / EULAR (21) và Mỹ (22), 32 trường hợp cá biệt khác đã được báo cáo. Có 22 trường hợp thuyên giảm lâm sàng. Khoảng 30% bệnh nhân đã giảm mức tái phát bệnh (23).
Với bệnh này, thời gian sau cấy ghép càng dài, nguy cơ tái phát càng cao. Điều này có liên quan đến mức độ kháng thể kháng dsDNA thấp trước khi có HSCT. Theo các nghiên cứu EBMT / EULAR, không có sự khác biệt về tần suất tái phát
- khi lựa chọn tế bào CD34 +
- hoặc với chế độ điều hòa cường độ cao hơn.
Đánh giá
Các tác dụng phụ của việc điều trị không nghiêm trọng. Và bệnh có thể được kiểm soát bằng các liệu pháp mà bệnh nhân đã kháng trước đó (21,22).
Có nhiều ví dụ về sự cải thiện lâm sàng ở những bệnh nhân bị SLE trải qua liệu pháp AHSCT hoặc điều trị bằng CY liều cao (24). Tuy nhiên, các quá trình viêm và tự miễn dịch mới đã xảy ra
- ở những bệnh nhân nộp HSCT (21),
- và ở những bệnh nhân chỉ được điều trị bằng CY mà không truyền tế bào gốc (24).
Điều này có thể xảy ra do sự xóa bỏ các tế bào T điều hòa (21).
Ngoài ra
Tại Brazil, bốn trường hợp SLE đầu tiên
- xin được điều trị bằng AHSCT trong một thử nghiệm hợp tác đa trung tâm,
- đã được báo cáo vào năm 2003 (1).
Các bệnh nhân được tiêm CY và ATG liều cao
Cả hai đều được dùng trước và sau khi truyền tế bào. Việc sử dụng ATG ngay sau truyền nhằm mục đích bổ sung cho quá trình xóa tế bào T in vivo. Vì trong quy trình, các tế bào được truyền không bị tổn thương. Ba bệnh nhân có biểu hiện suy thận nặng và 1 bệnh nhân tử vong.
3 bệnh nhân sống sót thuyên giảm bệnh thận sau cấy ghép
Nhưng 1 bệnh nhân tái phát sau đó. Và họ có dấu hiệu suy giảm chức năng thận (Scheinberg M, thông tin cá nhân). Bốn bệnh nhân khác được đưa vào thử nghiệm lâm sàng. 1 bệnh nhân không thể huy động tế bào gốc của mình và quay trở lại phương pháp ức chế miễn dịch thông thường. Và 3 bệnh nhân tử vong do biến chứng cấy ghép (suy thận cấp và nhiễm trùng máu) (20).
Một số nghiên cứu trong các tài liệu quốc tế đã chỉ ra rằng AHSCT có thể giảm bệnh SLE kháng thuốc. Cấy ghép có thể
- thay đổi tình trạng bệnh,
- làm cho chúng lành tính hơn,
- và đáp ứng tốt hơn với liệu pháp.
Có ý kiến cho rằng tỷ lệ tử vong cao hơn được báo cáo ở Brazil và các quốc gia khác (25) có thể được kiểm soát bằng cách
- lựa chọn bệnh nhân thích hợp,
- lựa chọn chế độ điều trị ít tích cực hơn,
- và thu thập thêm kinh nghiệm trong việc quản lý các biến chứng cụ thể liên quan đến thủ thuật (21).
3.3. Bệnh đa xơ cứng
Đặc trưng
Bệnh đa xơ cứng là
- một bệnh AD đặc hiệu,
- xuất hiện do tế bào T trung gian được kích hoạt chống lại các thành phần myelin trong hệ thần kinh trung ương (CNS).
Tiến triển
Sau phản ứng viêm thần kinh trung ương, quá trình khử myelin và mất sợi trục có thể xảy ra. Việc này dẫn đến gián đoạn tín hiệu điện. Hầu hết các bệnh nhân MS có biểu hiện tái phát và cải thiện từng đợt, được gọi là MS tái phát-thuyên giảm. Sau đó một giai đoạn được gọi là MS tiến triển thứ phát. Có một dạng MS khác được gọi là MS tiến triển nguyên phát, thường kháng các liệu pháp thông thường (26).
Các phương pháp điều trị MS có sẵn không thể chữa khỏi. Chúng có thể
- làm giảm viêm thần kinh trung ương,
- và trì hoãn tiến triển bệnh,
nhưng việc kiểm soát bệnh thường không đạt yêu cầu.
Việc sử dụng tế bào gốc trong điều trị MS
- dựa trên tác dụng ức chế miễn dịch và điều hòa miễn dịch AHSCT,
- có thể giúp cân bằng miễn dịch (26).
Vấn đề
Hơn nữa, tính chất đa tiêu điểm MS làm cho việc tiêm tế bào gốc vào từng vị trí bị ảnh hưởng không thể thực hiện được. Việc tiêm tĩnh mạch tế bào gốc có thể là một giải pháp thay thế MS và các tình trạng viêm thần kinh khác. Trong đó hàng rào máu não hematoencephalic có tính thẩm thấu trong các khu vực viêm.
Hơn thế nữa, AHSCT được báo cáo đầu tiên ở bệnh nhân MS được thực hiện vào năm 1995 (26). Đến tháng 11 năm 2002, MS là bệnh AD có số lượng báo cáo AHSCT lớn nhất. Hơn 200 bệnh nhân điều trị MS (3). Trên thực tế, tất cả các bệnh nhân đều trong giai đoạn MS tiến triển. Và hầu hết trong số họ đang trong giai đoạn MS tiến triển thứ phát.
Đánh giá
Những bệnh nhân này đã không đáp ứng với các phương pháp điều trị thông thường trước đó và bị mất chức năng nghiêm trọng. Không có sự khác biệt trong kết quả từ các trung tâm cấy ghép khác nhau (27). AHSCT làm giảm đáng kể tình trạng viêm thần kinh trung ương,
- như được thể hiện bằng hình ảnh cộng hưởng từ,
- và nâng cao kết quả thu được nhờ các liệu pháp thông thường (26).
Thách thức
Tác dụng phụ thường gặp nhất là nhiễm trùng, ảnh hưởng đến hơn 50% bệnh nhân trong thử nghiệm lâm sàng của Fassas và cộng sự (27). Tỷ lệ tử vong liên quan đến cấy ghép cao (5-10%) khi so sánh với điều trị thông thường (0%). Mặc dù người ta tin quy trình lựa chọn bệnh nhân nếu chính xác, tỷ lệ này có thể giảm xuống. Tỷ lệ mắc bệnh và tử vong dường như liên quan đến
- cường độ loại bỏ tế bào T và chế độ điều hòa,
- cũng như tuổi cao và mất chức năng nghiêm trọng (26).
Lưu ý
Cần phải xác định mức độ rủi ro có thể chấp nhận được ở những bệnh nhân mắc một căn bệnh, mặc dù nặng và hiếm khi có thể chữa khỏi, nhưng có tỷ lệ tử vong thấp.
Một số nghiên cứu lâm sàng đã báo cáo sự tồn tại của chứng teo não sau điều trị MS
Tuy nhiên, người ta vẫn chưa thể biết liệu AHSCT có ảnh hưởng gì đến việc teo não tiến triển hay không. Vì những bệnh nhân tham gia các nghiên cứu này mắc MS nặng và tiến triển nhanh chóng. Trong tình huống này, teo não có thể diễn ra với tốc độ nhanh.
Hơn nữa, giai đoạn bệnh tích cực hơn có thể xảy ra trong quá trình điều trị trước, chủ yếu là trong quá trình vận động tế bào. Theo đó, việc mất mô não có thể là hậu quả lâu dài của tình trạng bệnh. Hơn nữa, có khả năng bệnh nhân bị teo cơ giả, xảy ra để phản ứng với sự ức chế mạnh mẽ của bệnh do AHSCT gây ra (28).
Thách thức
AHSCT dường như không mang lại kết quả tốt ở những bệnh nhân thoái hóa sợi trục. Do đó, việc sử dụng AHSCT trong giai đoạn đầu của MS có vẻ phù hợp hơn cho những bệnh nhân có mức độ mất chức năng thấp (26).
Matrix metalloproteinase-9 (MMP-9), một dấu hiệu của cơ chế bệnh sinh MS
Chúng được điều chỉnh bởi chất ức chế mô của MMP-1. Huyết thanh và mức độ biểu hiện mRNA của MMP-9 và chất ức chế mô của MMP-1 được phân tích trong các tế bào đơn nhân ngoại vi từ 14 bệnh nhân bị MS sau AHSCT. Các kết quả chỉ ra sự ức chế hoạt động của MMP-9, phù hợp với tình trạng lâm sàng và giảm triệu chứng bệnh (33).
Cơ chế mà AHSCT ảnh hưởng đến tiến trình của MS vẫn chưa được biết
Hiệu quả tức thì dường như loại bỏ các bản sao tự động phản ứng. Bệnh nhân được điều trị bằng AHSCT có số lượng tế bào T CD4 + thấp (33). Và do đó, quá trình viêm giảm và có thể cải thiện chức năng lâm sàng. Bên cạnh tác dụng tức thì này, việc truyền tế bào gốc sau ức chế miễn dịch liều cao dường như làm phát sinh một hệ thống dung nạp “mới” (34). Một giả thuyết khác để giải thích sự cải thiện của bệnh nhân là
- khả năng của tế bào gốc để chuyển hóa thành các tế bào thần kinh đệm,
- và tiền chất tế bào thần kinh, góp phần sửa chữa các mô thần kinh bị tổn thương.
Do đó, AHSCT có thời gian ổn định kéo dài hoặc thay đổi mức độ bệnh.
3.4. Xơ cứng hệ thống
Đặc trưng
Bệnh xơ cứng bì hay xơ cứng bì hệ thống được đặc trưng bởi
- sự hoạt hóa tế bào T chiếm ưu thế,
- sản xuất kháng thể (chống xơ cứng bì-70),
- và tiết cytokine, dẫn đến xơ hóa quá mức khắp cơ thể.
Tiến triển
Các thể nặng của bệnh làm tăng tỷ lệ mắc và tử vong cao (ước tính khoảng 40-50% trong 5 năm). Giai đoạn thứ phát liên quan đến phổi, tim và thận. Các liệu pháp thông thường dường như không hiệu quả trong việc ngăn chặn sự tiến triển của bệnh và đảo ngược xơ hóa (35).
Vào tháng 11 năm 2003, 83 trường hợp bệnh nhân SS xin ghép tế bào gốc đã được đăng ký ở Châu Âu và Hoa Kỳ (35). Các chế độ điều trị được sử dụng để điều trị SS có ASCT được đăng ký trong EBMT / EULAR tương tự. Để huy động tế bào, việc sử dụng CY và G-CSF chỉ được ưu tiên hơn là chỉ sử dụng G-CSF. Việc chọn lọc tế bào CD34 + trước khi truyền lại được thực hiện ở 87% bệnh nhân. Đối với điều trị, CY được áp dụng trong 90% trường hợp, dưới dạng đơn trị liệu hoặc kết hợp ATG (36).
Lược sử
Từ năm 1996 nghiên cứu đạt kết quả tốt. Trong một nghiên cứu được công bố vào năm 2006, bao gồm 6 bệnh nhân bị SS, 1 trong số họ bị SLE liên quan, sự cải thiện được báo cáo về bệnh xơ cứng da ở tất cả các bệnh nhân (37).
Trong một nghiên cứu của Farge và cộng sự (36), 57 bệnh nhân SS đã được điều trị bằng HSCT trong giai đoạn từ 1996 đến 2002 và theo dõi trong hơn 6 tháng. Sự thuyên giảm hoàn toàn được quan sát thấy ở 14 bệnh nhân. Và thuyên giảm một phần ở 32 bệnh nhân, trong thời gian hơn 3 năm. Mặc dù một số bệnh nhân có biểu hiện bệnh tiến triển sau HSCT, họ được phát hiện có tình trạng lâm sàng tốt hơn so với trước điều trị.
Vấn đề
Tuy nhiên, không phải tất cả các kết quả được báo cáo đều thuận lợi. Trong một nghiên cứu đa trung tâm của Pháp với 11 bệnh nhân, trong khi phản ứng hoàn toàn hoặc một phần được quan sát ở 8 bệnh nhân, 5 trong số những bệnh nhân này cho thấy sự tái hoạt của bệnh. Tuy nhiên, theo các tác giả, AHSCT có thể kéo dài tuổi thọ ngắn của bệnh nhân SS nặng (36).
Các yếu tố độc tính không được phân tích toàn bộ do
- số lượng bệnh nhân ít,
- và do sự đa dạng của các phác đồ được áp dụng.
Điều trị bằng liều cao thuốc ức chế miễn dịch dường như ít được dung nạp hơn ở những bệnh nhân bị tổn thương phổi và tim do độc tính trên tim của CY. Việc lựa chọn bệnh nhân cẩn thận, theo dõi chặt chẽ trong quá trình điều trị và những thay đổi trong phác đồ ghép tạng làm giảm số ca tử vong (35). Chế độ điều hòa sử dụng thiotepa và liều thấp CY dường như
- giảm thiểu độc tính trên tim do CY gây ra (38),
- và khuyến cáo nên tránh dùng TBI trong trường hợp không có tác dụng bảo vệ phổi.
Đặc biệt
Được EBMT và EULAR giám sát, một nghiên cứu giai đoạn III ngẫu nhiên và có đối chứng đang được tổ chức, được gọi là Thử nghiệm quốc tế về cấy ghép tế bào gốc tự thân (3). Tại Hoa Kỳ, một nghiên cứu giai đoạn III ngẫu nhiên tương tự, được gọi là Xơ cứng bì: Cyclophosphamide hoặc Cấy ghép, đang được lên kế hoạch. Mục đích của những nghiên cứu này
- để khảo sát tác động của ức chế miễn dịch tăng cường sau HSCT,
- so sánh hóa trị liệu thông thường với CY ở bệnh nhân xơ cứng bì để thiết lập một phác đồ an toàn và hiệu quả hơn (35).
Điển hình
Trong thử nghiệm hợp tác của Brazil về AHSCT cho bệnh AD, bảy bệnh nhân mắc chứng SS tiến triển và khó chịu đã được điều trị (20). Ba bệnh nhân được huy động nhưng không được ghép (2 người cải thiện và 1 người tử vong do nhiễm trùng). Một bệnh nhân bị hội chứng chồng chéo (SLE cộng với SS) đã chết do bệnh tái hoạt (viêm mạch máu phổi và não) trước khi nhận HSCT. Ba bệnh nhân đã cải thiện đáng kể sau khi cấy ghép (làm mềm da và ổn định chức năng phổi). Nhưng 1 trong số họ đã chết vì nhiễm trùng phổi hơn 2 năm sau khi cấy ghép.
Sau báo cáo này, 2 bệnh nhân khác đã được cấy ghép tại Bệnh viện Đại học São Paulo ở Ribeirão Preto mà không có biến chứng sớm và các tổn thương da được cải thiện nhanh chóng.
3.5. Tế bào bạch cầu tự miễn
Đặc trưng
Ban xuất huyết giảm tiểu cầu tự miễn (AITP) là
- một bệnh trong đó các tiểu cầu bị nhạy cảm bởi các kháng thể chống tiểu cầu,
- hoặc các phức hợp miễn dịch lưu hành,
- kích thích việc loại bỏ sớm các tế bào này khỏi hệ tuần hoàn.
Tiến triển
Quá trình này dẫn đến giảm tiểu cầu và chảy máu. Khoảng một phần ba bệnh nhân AITP không đáp ứng tốt với các liệu pháp thông thường. Liều cao của thuốc ức chế miễn dịch có thể giúp thuyên giảm bệnh. Tuy nhiên, điều này kéo theo những rủi ro liên quan đến suy tủy. HSCT nhằm mục đích đẩy nhanh việc thiết lập lại các thông số huyết học. Đồng thời làm giảm số lượng tế bào tự miễn dịch trong cơ thể (39).
Một số báo cáo trường hợp lẻ tẻ về HSCT đối với các tế bào miễn dịch tự miễn đã được công bố. Nhưng chỉ có hai nghiên cứu được báo cáo với số lượng bệnh nhân vừa phải.
Điển hình
Một nghiên cứu đã mô tả tiền sử lâm sàng của những bệnh nhân đăng ký EBMT đã được điều trị bằng HSCT để điều trị chứng giảm tế bào tự miễn dịch nặng. Trong 12 bệnh nhân có AITP được gửi để cấy ghép tự thân, các phản ứng rất đa dạng, thay đổi từ đáp ứng thoáng qua đến thuyên giảm liên tục hoặc thậm chí tử vong liên quan đến cấy ghép (40).
Tại Hoa Kỳ, trong số 14 bệnh nhân AITP mãn tính được điều trị bằng cyclophosphamide liều cao (200 mg / kg), tiếp theo là AHSCT, 6 bệnh nhân đạt được đáp ứng hoàn toàn bền vững và 2 đáp ứng một phần lâu bền (41).
Nghiên cứu kết luận rằng việc truyền HSC đã thúc đẩy quá trình tái lập huyết học. Vì cải thiện lâm sàng không liên quan đến việc định lượng kháng thể chống GPIb hoặc kháng GPIIIa, nên có khả năng các kháng nguyên tiểu cầu khác có liên quan đến AITP.+ tế bào được truyền vào bệnh nhân, mặc dù sự xóa bỏ tế bào lympho T có thể đã ngăn cản sự tái truyền của tế bào T phản ứng tự động (39).
Các thử nghiệm lâm sàng liên quan đến số lượng bệnh nhân lớn hơn có thể cung cấp
- thông tin đáng tin cậy hơn về tầm quan trọng của việc loại bỏ tế bào lympho,
- và đặc điểm di truyền miễn dịch của những bệnh nhân đáp ứng hoặc không đáp ứng với điều trị.
Sau đó, có thể so sánh các phác đồ điều trị khác nhau
- a) liệu pháp chỉ dựa trên CY liều cao;
- b) liệu pháp sử dụng CY liều cao kết hợp cấy ghép tế bào gốc,
- và c) quy trình sau này được sử dụng kết hợp với các tác nhân duy trì khả năng dung nạp sau ghép (39).
Thiếu máu tự miễn (AIHA) được xác định bởi sự phá hủy hồng cầu do sự cố định của globulin miễn dịch hoặc protein trên bề mặt màng tế bào. Các triệu chứng ban đầu có thể do
- thiếu máu,
- tác động thứ phát của tình trạng tan máu hoặc bệnh chính gây ra AIHA.
Có một vài báo cáo trong các tài liệu khoa học về các trường hợp cấy ghép tế bào gốc đã được sử dụng để điều trị AIHA (40,42). Và dữ liệu cho thấy các liệu pháp ức chế miễn dịch nên được sử dụng sau khi cấy ghép trong bệnh này.
Bất chấp những dữ liệu ban đầu, cấy ghép tế bào gốc mang lại một khả năng điều trị mới cho bệnh nhân AIHA.
3.6. Đái tháo đường
Vấn đề
Trong những năm gần đây, số ca mắc bệnh tiểu đường trên toàn thế giới tăng nhanh. Bệnh này ảnh hưởng đến khoảng 6-8% dân số thế giới và số lượng bệnh nhân mới được chẩn đoán tăng lên hàng năm (43). Trong số này, khoảng 10% là bệnh tiểu đường loại I. Bệnh đái tháo đường phụ thuộc insulin, một bệnh AD gây ra bởi sự phá hủy ngày càng tăng của các tế bào ß tuyến tụy tiết insulin (4,44) điều chỉnh lượng đường trong máu bằng cách tiết của insulin.
Dữ liệu lâm sàng gần đây cho thấy căn bệnh này có thể được chữa khỏi nếu được cung cấp đầy đủ các tế bào ß mới. Do đó, một mục tiêu của sinh học phát triển tuyến tụy là tìm hiểu cách thức tạo ra các tế bào ß nội sinh, với hy vọng sản xuất chúng một cách ngoại sinh (44).
Hứa hẹn
Cấy ghép tế bào tụy là một phương pháp điều trị hấp dẫn đối với bệnh tiểu đường loại I (45). Các thử nghiệm cấy ghép trên lâm sàng dựa trên các vùng tổn thương đã chứng minh rằng thực sự có thể khôi phục khả năng tiết insulin ở bệnh nhân tiểu đường loại I thông qua cấy ghép các tế bào sản xuất insulin (46). Có một số khó khăn liên quan đến việc cấy ghép liên quan đến
- tính miễn dịch,
- tự miễn dịch,
- và nhu cầu về khối lượng tế bào đảo nhỏ hơn.
Ý tưởng
Việc sử dụng tế bào gốc làm nguồn sản xuất insulin thay thế được xem xét để giải quyết vấn đề thiếu hụt mô người (45). Liệu pháp ức chế miễn dịch suốt đời và không đủ nguồn đã hạn chế lợi ích của cấy ghép tiểu đảo xuống dưới 0. 5% bệnh nhân tiểu đường loại I. Trong nguy cơ tiềm ẩn của sự lây nhiễm bởi vi rút động vật nội sinh hạn chế
- việc sử dụng phương pháp cấy ghép đảo nhỏ,
- việc lấy các tế bào gốc dường như có thể khắc phục được các vấn đề thiếu hụt mô và khả năng tương thích miễn dịch (4).
Thực nghiệm
Thực tế là BM chứa HSC và MSC, có khả năng biệt hóa thành một số loại tế bào khác nhau như tế bào tuyến tụy, trong những năm gần đây, đã khuyến khích nghiên cứu điều trị bệnh tiểu đường loại I. Tuy nhiên, có một số tranh cãi liên quan đến kết quả thu ESC và ASC, nó
- liên quan đến khả năng tiết insulin trong ống nghiệm,
- và bình thường hóa cơ chế in vivo tăng đường huyết (4).
Sự thật
Tế bào gốc từ lá lách đã được chứng minh là nơi chúng trưởng thành thành các tế bào chức năng phục hồi đường huyết (47).
Cấy ghép các tế bào sản xuất insulin có nguồn gốc từ ESC đã đẩy lùi bệnh tiểu đường ở động vật, cho thấy rằng các tế bào này tổng hợp và giải phóng insulin. Các thí nghiệm trên chuột mắc bệnh tiểu đường với các tế bào ß bị phá hủy hoàn toàn bởi streptozocin cho thấy sau ghép BMT, đường huyết trở lại bình thường và thời gian sống sót lâu hơn (4).
Xu hướng
Một nghiên cứu gần đây đã chứng minh khả năng của các tế bào gan người trưởng thành được nuôi cấy như các tế bào sinh trưởng của tuyến tụy, cho thấy tính dẻo của các tế bào gan chưa trưởng thành. Khả năng sử dụng gan như một mô tiền thân của tuyến tụy đã được chứng minh ở chuột Xenopus và người.
Việc sử dụng tế bào gan người trưởng thành để tạo mô sản xuất insulin chức năng có thể mở đường cho việc cấy ghép mô tự thân. Do đó nó cho phép bệnh nhân tiểu đường trở thành người hiến tặng mô sản xuất insulin của chính mình (43).
Nhấn mạnh
Tế bào gốc mang lại cơ hội tốt nhất để đạt mục tiêu này. Các kết quả gây tranh cãi đã được trình bày liên quan đến sự tồn tại và bản chất của tế bào gốc hoặc tế bào tiền thân của đảo tụy (46). Cũng có tranh cãi liên quan đến kết quả thu được ở ESC và ASC trong quá trình tiết insulin trong ống nghiệm và bình thường hóa việc tăng đường huyết trong cơ thể.
Nghiên cứu ESC có tiềm năng phát triển hơn nghiên cứu ASC. Tuy nhiên nó vẫn đang trong giai đoạn nghiên cứu cơ bản. Các dòng ESC hiện tại không giống nhau hoặc lý tưởng để tạo ra các tế bào tiết insulin hoặc tế bào ß và các dòng ESC bổ sung phải được thiết lập (4).
HSC chimerism đạt được thông qua BMT có thể ảnh hưởng đến bệnh tiểu đường loại I theo hai cách:
- thứ nhất, bằng cách gây khả năng dung nạp ở tuyến tụy,
- và thứ hai bằng cách đảo ngược quá trình tự miễn trước phát triển các biến chứng cuối (48).
Đánh giá
Những nghiên cứu này cho thấy BMT là một phương pháp điều trị để thay thế tế bào ß (4). Tuy nhiên, BMT dị sinh có những hạn chế bao gồm tỷ lệ mắc bệnh liên quan đến bệnh thải ghép vật chủ và thất bại trong quá trình kết hợp. Hiện tại, tỷ lệ mắc bệnh và tử vong liên quan đến bệnh điều hòa không thể được biện minh cho sự cảm ứng dung nạp hoặc gián đoạn trạng thái tự miễn dịch ở bệnh tiểu đường loại I (48).
Trong khi phá hủy miễn dịch là một vấn đề trong BMT, việc cấy ghép các tế bào trung mô lách đã mang lại kết quả đầy hứa hẹn trong cả việc tái tạo tế bào ß tuyến tụy và ngăn ngừa sự phá hủy miễn dịch (4).
Ghi nhận
Đã có những tiến bộ đáng kể trong điều trị bệnh tiểu đường loại I trong suốt thế kỷ qua, nhưng BMT là phương pháp duy nhất có khả năng làm gián đoạn và đảo ngược quá trình tự miễn dịch trước khi phát triển các biến chứng cuối.
Khi các hạn chế liên quan đến BMT thông thường được khắc phục, BMT có thể trở thành một lựa chọn điều trị trong điều trị bệnh đái tháo đường tự miễn dịch và cảm ứng dung nạp.
Các kỹ thuật hứa hẹn tạo điều kiện thuận lợi cho việc sử dụng BMT hiện đang được nghiên cứu, bao gồm
- việc phát triển các chiến lược điều hòa một phần,
- kỹ thuật ghép BM để làm giàu HSC và quần thể tế bào,
- tạo điều kiện cho quá trình kết hợp và các phương pháp hạn chế bệnh thải ghép vật chủ.
Lưu ý
Việc sử dụng các loại tế bào gốc khác nhau làm nguồn tái tạo tế bào ß cũng rất quan trọng, như đã được xem xét gần đây (49). Kết quả cuối cùng sẽ là BMT an toàn hơn,
Từ tháng 12 năm 2003 đến tháng 7 năm 2006, 15 bệnh nhân đái tháo đường týp I khởi phát sớm (chưa đến 6 tuần kể từ khi được chẩn đoán) đã nhận được giấy phép AHSCT tại Bệnh viện Đại học của Trường Y Ribeirão Preto, sử dụng CY (200 mg / kg) và ATG thỏ ( 4,5 mg / kg) như một chế độ điều hòa (50).
Trong số 14 bệnh nhân không bị nhiễm toan ceton trước đó và dùng steroid để điều trị,
- 12 bệnh nhân không còn insulin ngay sau khi cấy ghép,
- 2 bệnh nhân sau 1 năm kể từ khi cấy ghép,
- và 1 bệnh nhân tái phát sau khi nhiễm virus.
3.7. Teo cơ xơ cứng cột bên
Đặc trưng
Bệnh xơ cứng teo cơ bên (ALS) là
- một bệnh gây tử vong,
- xác định bởi cái chết của các tế bào thần kinh vận động trung ương và ngoại vi,
- dẫn đến rối loạn chức năng vận động nghiêm trọng (5,51).
Điển hình
Trong một số trường hợp, từ 5 đến 10%, nguồn gốc là do di truyền, rõ ràng là do đột biến gen superoxide dismutase (52). Nhưng trong hầu hết các trường hợp (ALS lẻ tẻ), nguyên nhân của bệnh không được biết rõ. Các bất thường về tự miễn và viêm có thể ảnh hưởng đến sự tiến triển của bệnh. Nhưng ALS không phải là bệnh AD điển hình. Chiến lược điều trị được sử dụng trong các trường hợp ALS liên quan đến việc cố gắng ngăn chặn sự mất tế bào thần kinh và kích thích tái tạo tế bào.
Hiện tại
Các liệu pháp kết hợp được thiết kế để ngăn chặn sự tiến triển của bệnh. Việc sử dụng các thuốc và thuốc bảo vệ thần kinh, có ảnh hưởng có ý nghĩa thống kê đến sự sống còn của bệnh nhân. Tuy nhiên, những liệu pháp này không có khả năng phục hồi chức năng vận động đã mất. Trong ALS, mục tiêu điều trị là cải thiện sự tương tác giữa tế bào thần kinh vận động và tế bào không phải tế bào thần kinh, chủ yếu là tế bào thần kinh đệm và tế bào vi mô. Liệu pháp tế bào gốc là một chiến lược đầy hứa hẹn để phục hồi chức năng vận động thần kinh và / hoặc ngăn ngừa thoái hóa tế bào thần kinh vận động trong trường hợp ALS (5).
Lược sử
Cho đến một vài năm trước, các nhà khoa học tin rằng mô tế bào thần kinh là không thể thay đổi. Tuy nhiên, bây giờ họ biết việc thay thế tế bào xảy ra ở tuổi trưởng thành ở một số vùng cụ thể của não. Khó khăn trong việc lấy tế bào gốc thần kinh trưởng thành đã dẫn đến việc sử dụng UCB và BM làm nguồn tế bào gốc thay thế trong liệu pháp điều trị ALS. Những tế bào này có thể tạo ra sự biệt hóa thành loại tế bào mong muốn và sau đó được cấy ghép (5).
Tiến hành
Quá trình chuyển hóa của HSC ở người từ UCB sang tế bào thần kinh đã được thử nghiệm trong ống nghiệm. Những tế bào này được biệt hóa thành tế bào thần kinh và tuần tự thành tế bào hình sao trong một vi môi trường thích hợp. Có những báo cáo cho thấy sự phân biệt ESCs thành tế bào thần kinh vận động ở chuột.
Tuy nhiên, khả năng của quá trình biệt hóa còn gây tranh cãi và các giải thích sinh học khác đã được đề xuất, đặc biệt là sự dung hợp tế bào. Cogle và các đồng nghiệp (6) đã chỉ ra sự biệt hóa của HSC ở người thành tế bào thần kinh, tế bào hình sao và tế bào vi mô khi không có sự dung hợp tế bào.
Trong một nghiên cứu khác, sau khi truyền ESC của người vào chất lỏng cephalorachidian (CRL) của chuột SOD1,
- các tế bào gốc di chuyển đến vùng bị tổn thương của tủy sống,
- và khoảng 6% trong số các tế bào được tiêm này đã tạo ra các tế bào thần kinh mới,
- và những con chuột được điều trị cải thiện tình trạng tê liệt (52).
Theo Svendsen và Langston (51), những kết quả này chủ yếu là do
- sự biệt hóa thành các tế bào thần kinh đệm,
- việc sản xuất các yếu tố dinh dưỡng bảo vệ thần kinh,
- chứ không phải do sự thay thế trực tiếp các tế bào thần kinh vận động.
Do hạn chế của quá trình biệt hóa tế bào, xu hướng ghép tế bào gốc thần kinh
- để biệt hóa thành các dòng tế bào thần kinh đệm sau cấy vào tủy sống,
- và khó khăn trong việc chuyển hóa tế bào máu người thành tế bào thần kinh trong ống nghiệm,
- liệu pháp dựa trên tế bào gốc trong ALS vẫn còn còn lâu mới được áp dụng.
Vấn đề
Tuy nhiên, nhu cầu điều trị của những bệnh nhân này đã dẫn đến các nghiên cứu lâm sàng, mặc dù không có bằng chứng kết luận. Trong một nghiên cứu lâm sàng, CD34 + tế bào được tinh chế từ máu ngoại vi được tiêm vào 3 bệnh nhân ALS. Sau 12 tháng, trong khi không có bệnh nhân nào cho thấy bất kỳ tác dụng phụ nghiêm trọng nào nhưng không có lợi ích lâm sàng rõ ràng nào.
Tuy nhiên, các nghiên cứu khác cho thấy kết quả hứa hẹn hơn. MSCs mở rộng được tiêm vào CRL của 7 bệnh nhân và 3 tháng sau khi cấy ghép, 4 người trong số họ có phản ứng lâm sàng tích cực (5).
Mục đích của việc ứng dụng tế bào gốc trong các trường hợp ALS là để
- đạt được sự biệt hóa của các tế bào này thành tế bào thần kinh vận động,
- và thiết lập các kết nối chức năng thích hợp.
Tế bào gốc cũng có thể
- hoạt động thông qua việc cung cấp các yếu tố dinh dưỡng và tăng trưởng,
- tạo ra một môi trường thuận lợi cho sự tồn tại của tế bào thần kinh,
- và hoạt động như chất bảo vệ chống lại các chất độc thần kinh (5).
Đánh giá
Hầu hết các nghiên cứu lâm sàng liên quan đến việc sử dụng liệu pháp tế bào trong các trường hợp ALS đều sử dụng phương pháp tiêm tế bào gốc tự thân hoặc ESCs trực tiếp vào thần kinh trung ương. Janson và cộng sự (53 tuổi), sau khi thử kỹ thuật này ở động vật linh trưởng, đã tiêm HSCs (tế bào CD34 +) được chọn vào khoang nội tủy của 3 bệnh nhân.
Các tác giả đã quan sát thấy các tác động một phần hoặc nhẹ lên chức năng thần kinh và không có biến chứng
Trong một nghiên cứu khác được thực hiện tại Đại học Turin, Ý (54), 7 bệnh nhân bị mất khả năng vận động chi dưới nhưng không có triệu chứng hô hấp, đã nhận được liệu pháp ex vivo mở rộng. Hầu hết các bệnh nhân thấy các tác dụng phụ nhẹ và có thể hồi phục (đau cơ liên sườn hoặc rối loạn cảm giác), kết quả được xác nhận sau 2 năm theo dõi (55).
Tình trạng giảm tốc độ mất sức mạnh cơ bắp ở chân được quan sát thấy 3 tháng sau khi cấy ghép ở 4 bệnh nhân cùng việc cải thiện nhẹ ở 2 bệnh nhân (54). Ngoài ra, sự suy giảm chức năng hô hấp cũng giảm nhanh ở 4 bệnh nhân sau 2 năm. Những tác động này tương quan với số lượng tế bào được tiêm (55).
Ngoài ra
Tại một sự kiện khoa học (56), một báo cáo đã được trình bày về việc sử dụng các tế bào gốc chiết xuất phôi thai 4 đến 8 tuần được tiêm vào 61 bệnh nhân mắc ALS từ 1 đến 4 lần. Cải thiện chức năng thần kinh được báo cáo ở 34% bệnh nhân sau 2 tháng. Và sau đó, ở những bệnh nhân được tiêm lặp lại.
Các phát hiện cho thấy kết quả tốt hơn ở những trường hợp bệnh ở giai đoạn sớm hơn, nhưng không có dữ liệu nào về khả năng sống sót. Một nhà nghiên cứu từ Montevideo, Uruguay, đã điều trị cho 12 bệnh nhân ALS bằng HSC được thu thập từ máu ngoại vi, lơ lửng trong CRL và tiêm trực tiếp vào tủy sống. Kết quả khá đáng khích lệ, vì chức năng thần kinh được cải thiện ở 3 bệnh nhân và ổn định ở mức 9 (57).
Hiện trạng
Có rất ít báo cáo về việc sử dụng HSCT, sau đó là ức chế miễn dịch liều cao ALS. Một báo cáo đã được gửi đến Cơ quan đăng ký HSCT Châu Âu về bệnh AD (EBMT / EULAR, có trụ sở tại Basle, Thụy Sĩ) của 2 bệnh nhân được gửi đến AHSCT ở Pháp (Tyndall A, thông tin liên lạc cá nhân). Mặc dù có sự cải thiện nhất thời trong thời gian 3 tháng ở một trong số các bệnh nhân, cả hai đều chết khoảng 7 tháng sau cấy ghép.
Tại Mỹ, một nhóm các nhà khoa học từ Đại học Y khoa Baylor, Houston, TX, đã thực hiện một nghiên cứu thí điểm liên quan đến 6 bệnh nhân ở các giai đoạn trung gian của bệnh, những người nhận được BMT dị sinh từ anh chị em giống HLA của họ (58). Tất cả các bệnh nhân đều được ghép tế bào hiến tặng và 3 bệnh nhân không cho thấy lợi ích gì từ thủ thuật này, trong đó 2 người tử vong và bệnh tiếp tục tiến triển ở người còn lại.
Tuy nhiên, 3 bệnh nhân còn lại có biểu hiện giảm bệnh. Khám nghiệm tử thi 1 trong số các bệnh nhân cho thấy số lượng lớn DNA của người hiến tặng ở các vùng khác nhau của tủy sống và não, chứng tỏ rằng các tế bào BM đồng sinh có khả năng vượt qua hàng rào máu não và tự kết hợp vào mô thần kinh.
Tổng thuật
Có bằng chứng cho thấy quá trình viêm là một yếu tố chính trong cơ chế bệnh sinh của ALS (59) và ức chế miễn dịch liều cao với cấy ghép tế bào gốc có thể thay đổi lịch sử tự nhiên của bệnh (60). Dựa trên bằng chứng này, AHSCT cho ALS bắt đầu ở Brazil vào tháng 12 năm 2004 tại Bệnh viện Đại học của Trường Y Ribeirão Preto. Hai bệnh nhân được cấy ghép bằng phác đồ ức chế miễn dịch bộ ba (CY, ATG và fludarabine).
Ghi nhận
Người đầu tiên chết do thuyên tắc phổi. Và người thứ hai vẫn còn sống 28 tháng sau khi cấy ghép. Một kinh nghiệm sâu rộng hơn về AHSCT đã có được tại Bệnh viện Salvador ở Bahia, nơi 15 bệnh nhân được cấy ghép bằng cách sử dụng cùng một chế độ điều hòa. Có 3 trường hợp tử vong liên quan đến cấy ghép. 1 trường hợp tử vong liên quan đến chứng tiến triển. Và 1 bệnh nhân đột tử không liên quan đến cấy ghép.
Mười bệnh nhân còn sống sau thời gian theo dõi trung bình 133 ngày (1-540) (Pallotta R, giao tiếp cá nhân). Cả hai quy trình đã bị hội đồng CONEP tạm dừng trong khi chờ sửa đổi.
4. Phần kết luận
Một trong những cách trị bệnh tự miễn được đánh giá cao là cấy ghép tế bào gốc. Vì nó có tác dụng ức chế miễn dịch và điều hòa miễn dịch.
Việc cấy ghép tế bào gốc có thể
- phá hủy hệ miễn dịch bị lỗi,
- làm mới hệ thống bạch huyết,
- giảm hoạt động của bệnh,
- và dẫn đến việc thuyên giảm bệnh AD lâu dài (27).
Những bệnh nhân AD đã từng kháng liệu pháp thông thường, sau cấy ghép,
- đã trở nên nhạy cảm với cùng liệu pháp thông thường,
- làm nổi bật các đặc tính điều hòa miễn dịch của việc cấy ghép tế bào gốc.
Đặc trưng
Hầu hết các nghiên cứu lâm sàng dựa trên liệu pháp tế bào gốc ở bệnh nhân AD sử dụng AHSCT được huy động từ BM đến máu ngoại vi. Không có sự khác biệt đáng kể trong các quy trình cấy ghép được sử dụng cho các bệnh khác nhau. Các kết quả được tổng quan này bao gồm
- các trường hợp thuyên giảm hoàn toàn hoặc một phần,
- tái phát hoặc ổn định bệnh
- tiến triển bệnh và tử vong.
Lời khuyên
Việc lựa chọn bệnh nhân dường như ảnh hưởng trực tiếp đến kết quả cấy ghép. Việc lựa chọn bệnh nhân trong giai đoạn đầu của bệnh dường như an toàn và hiệu quả hơn. Tuy nhiên, quy trình này có nguy cơ khiến những bệnh nhân có thể đáp ứng tốt liệu pháp thông thường và các phương pháp điều trị không chuẩn mới (21). Hầu hết các quy trình được xem xét ở đây được thực hiện ở những bệnh nhân không đáp ứng các liệu pháp điều trị thông thường. Ở những bệnh nhân như vậy, việc sử dụng tế bào gốc, mặc dù vẫn còn là một quy trình thử nghiệm, nhưng mang lại một cơ hội mới để nâng cao chất lượng cuộc sống.
Tồn tại
Có một số tranh cãi liên quan đến việc sử dụng hóa trị liều cao trong trường hợp không truyền tế bào gốc, mà trong một số trường hợp, đã dẫn đến kết quả khả quan, cho thấy việc ức chế miễn dịch có thể là nguyên nhân thực sự của sự cải thiện bệnh (26). Ngoài ra, tổng số bệnh nhân được đánh giá trong một số nghiên cứu khá nhỏ. Vì các báo cáo trường hợp nhỏ không được kiểm soát. Ngoài ra, các cá thể đại diện cho nguồn gốc di truyền
- rất đa dạng,
- và chỉ các thử nghiệm lâm sàng ngẫu nhiên theo quy trình tiêu chuẩn mới cho phép chúng tôi đưa ra kết luận có ý nghĩa.
Hơn nữa, cần có các nghiên cứu đánh giá việc
- sử dụng các liệu pháp duy trì sau cấy ghép,
- xác định các quy trình lựa chọn bệnh nhân,
- và đánh giá việc huy động tế bào gốc trong điều trị bệnh AD.
Bệnh nhân tái phát phổ biến hơn trong cấy ghép tự thân (30%) so với cấy ghép đồng loại (5%). Và sau đó nó cũng cho kết quả lâu dài hơn (26). Việc tái phát có thể do
- ô nhiễm các tế bào tự miễn,
- mất khả năng điều hòa tiêu diệt các tế bào miễn dịch gây ra bệnh,
- hoặc sự hiện diện của khiếm khuyết trong quá trình nhân rộng tế bào gốc (14).
Việc ô nhiễm mô ghép bởi các tế bào lympho phản ứng tự động có thể được kiểm soát bằng cách sử dụng các dòng tế bào thuần khiết được mở rộng trong phòng thí nghiệm. Điều này cũng làm tăng số lượng tế bào gốc có sẵn cho bệnh nhân (26). Hiệu quả của việc cấy ghép dị gen chủ yếu là
- kết quả của sự thay đổi tính nhạy cảm di truyền của vật chủ đối với bệnh,
- và cũng liên quan đến hiệu ứng ghép so với bệnh.
Hiện tại,
Các nhà khoa học đã biết ESCs có khả năng biệt hóa lớn hơn và ít tiềm năng di truyền miễn dịch hơn ASC. Tuy nhiên, ESC có thể được sử dụng như một giải pháp thay thế khi có nguy cơ cao bị từ chối miễn dịch, như
- trong trường hợp cấy ghép đồng gen,
- hoặc trong trường hợp tái phát do hệ quả của kiểu gen bệnh nhân,
- như xảy ra trong việc cấy ghép tự thân.
Tuy nhiên,
- việc sử dụng ESCs vẫn còn hạn chế,
- và chưa thể trở thành một phương pháp điều trị thay thế cho những bệnh nhân này do nguy cơ phát triển u quái,
- và các vấn đề đạo đức liên quan đến việc sử dụng thủ thuật này.
Đánh giá
MSCs là một cách trị bệnh tự miễn đầy hứa hẹn. Các tế bào này có đặc tính ức chế miễn dịch. Và có báo cáo cho thấy mức độ biểu hiện phân tử HLA trong MSCs thấp. Các nhà khoa học tin rằng liệu pháp trung gian tế bào trung mô có thể cho phép
- tiết ra các yếu tố ức chế miễn dịch,
- và có thể sửa chữa các mô bị phá hủy bởi quá trình viêm mãn tính.
Xu hướng
Một cách tiếp cận cách trị bệnh tự miễn hỗn hợp bao gồm
- sự kết hợp giữa chuyển gen với liệu pháp tế bào
- có thể làm tăng hiệu quả điều trị của việc cấy ghép tế bào gốc.
Nó cho phép
- điều chỉnh các dị thường di truyền,
- và giúp kiểm soát bệnh tật bằng cách tăng sự biểu hiện của các yếu tố điều tiết (21).
Trong các bệnh thoái hóa thần kinh, các tế bào gốc thần kinh có thể
- vẫn ở giai đoạn tĩnh lặng
- do môi trường vi mô không thuận lợi do bệnh gây ra.
Các nhà khoa học tin các tế bào gốc biến đổi gen có thể
- kích thích sự gia tăng của các tế bào gốc nội sinh,
- và do đó dẫn đến việc sửa chữa vùng thần kinh bị tổn thương (5).
Một chiến lược thú vị gắn nhãn các tế bào gốc được truyền để đánh giá sau này về
- sự tăng sinh,
- biệt hóa,
- di chuyển,
- và di chuyển của chúng.
Việc ghi nhãn tế bào, chẳng hạn như đã đạt được bởi Cogle và các đồng nghiệp (6),
- giúp mở rộng kiến thức có sẵn về hoạt động và sinh học của tế bào gốc,
- để đánh giá hiệu quả của việc cấy ghép,
- và phát triển các quy trình tốt hơn để ứng dụng tế bào gốc từng bệnh lý miễn dịch.
Cách trị bệnh tự miễn bằng tế bào gốc đầy hứa hẹn. Một số báo cáo đã phân tích những lợi ích tiềm năng của việc cấy ghép tế bào gốc. Hy vọng, các nghiên cứu mới cho kết quả tốt cho việc điều trị bệnh AD trong tương lai gần.
Xem thêm bài viết
- Liệu pháp ozone và bệnh ung thư: Những thông tin căn bản cần biết
- Liệu pháp ozone và bệnh ung thư: Những thông tin căn bản cần biết
- Liệu pháp ozone cho bệnh Lyme và những rủi ro khoa học đã chứng minh
Nguồn: Tổng hợp







![[Bật mí] Phòng khám Đa khoa Việt Mỹ ở Gò Vấp có tốt không? 6 Phòng khám Đa khoa Việt Mỹ](https://songkhoe.medplus.vn/wp-content/uploads/2022/03/1590826139931.png)


![[Review] Phòng khám đa khoa Âu Á ở Hồ Chí Minh có tốt không? 9 Phòng khám đa khoa Âu Á](https://songkhoe.medplus.vn/wp-content/uploads/2022/03/phong-kham-da-khoa-o-tphcm-au-a.jpg)


![[TOP 10] bài viết về Barrett thực quản hay 2022 12 [TOP 10] bài viết về Barrett thực quản hay 2022](https://songkhoe.medplus.vn/wp-content/uploads/2022/11/TOP-10-bai-viet-ve-Barrett-thuc-quan-hay-2022.png)