Thuốc Tavin-EM là gì?
Thuốc Tavin-EM là thuốc ETC dùng sử dụng điều trị nhiễm HIV-1 ở người lớn.
Tên biệt dược
Thuốc được đăng ký dưới tên Tavin-EM
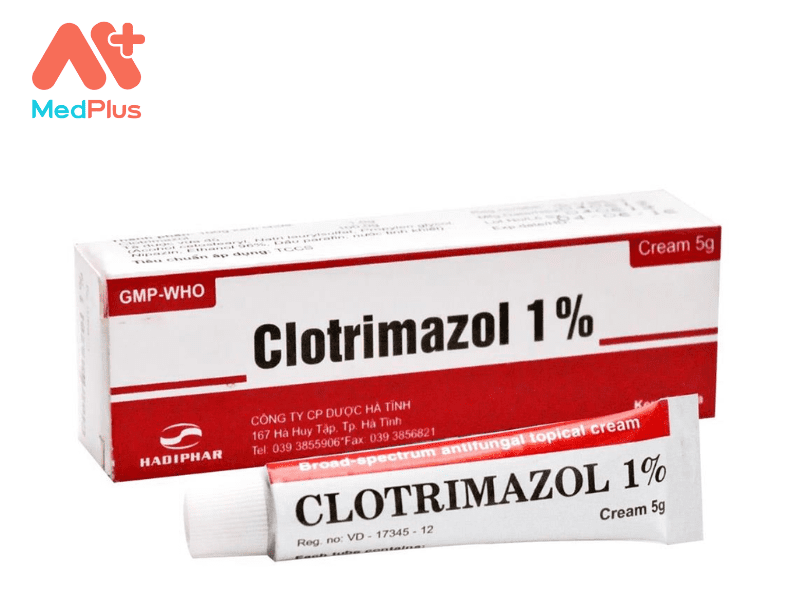
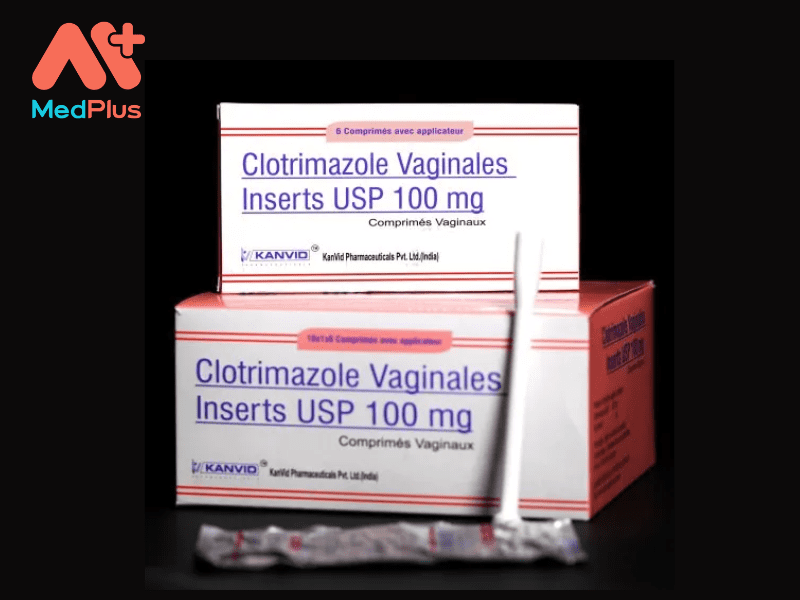
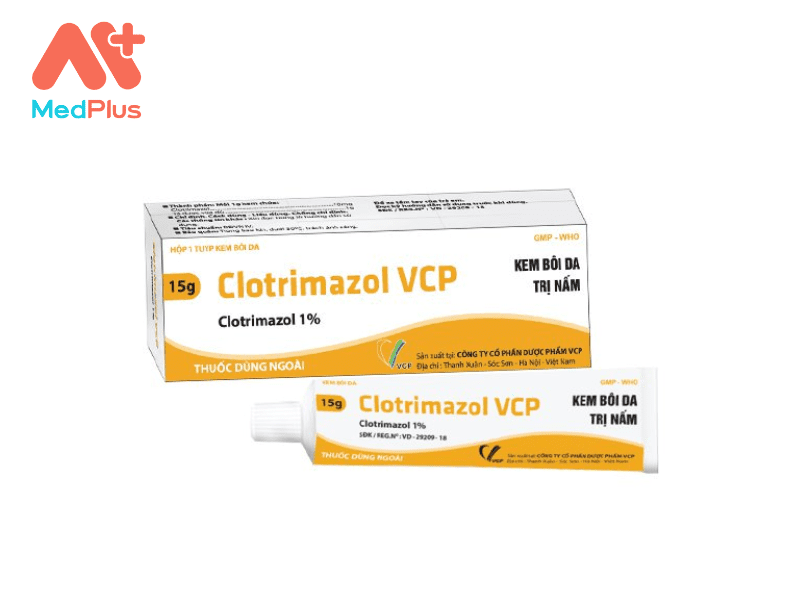
Dạng trình bày
Thuốc được bào chế dưới dạng viên nén bao phim
Quy cách đóng gói
Thuốc được đóng gói ở dạng: hộp 1 chai 30 viên
Phân loại thuốc Tavin-EM
Thuốc Tavin-EM là thuốc ETC – thuốc kê đơn
Số đăng ký
Thuốc có số đăng ký: VN3-71-18
Thời hạn sử dụng
Thuốc có hạn sử dụng là 24 tháng kể từ ngày sản xuất.
Nơi sản xuất
Thuốc được sản xuất ở: Emcure Pharmaceuticals Ltd.
Địa chỉ: Lane No. 3. Phase-II, SIDCO Industrial Complex Bari-Brahmana, Jammu (J&K)-181133 Ấn Độ
Thành phần của thuốc Tavin-EM
- Tenofovir disoproxil fumarat: 300 mg
- Emtricitabin: 200 mg
- Tá dược: Croscarmellose natri, Pregelatinized starch, Lactose monohydrate, Cellulose vi tinh thể [PH 101], Cellulose vi tinh thể [PH102], Povidon [PVP K-30], Magnesi Stearat, Opadry white AMB 80W68912
Công dụng của thuốc Tavin-EM trong việc điều trị bệnh
Thuốc Tavin-EM là thuốc ETC dùng sử dụng điều trị nhiễm HIV-1 ở người lớn.
Hướng dẫn sử dụng thuốc Tavin-EM
Cách dùng thuốc Tavin-EM
Thuốc dùng qua đường uống
Liều dùng thuốc Tavin-EM
- Uống 1 viên thuốc mỗi ngày sau bữa ăn
- Nếu một liều Tavin – EM bị bỏ quên trong vòng 12 giờ, nên dùng Tavin-EM càng sớm càng tốt và tiếp tục lịch trình dùng thuốc bình thường.
- Nếu một liều của Tavin-EM bị bỏ qua hơn 12 giờ và gần như là thời gian cho liều tiếp theo, bạn có thể bỏ qua liều đã quên và tiếp tục lịch trình dùng thuốc của bạn. Không dùng liều gấp đôi đẻ bù cho liều bỏ lỡ.
- Nếu nôn mửa xảy ra trong vòng l giờ sau khi dùng thuốc Tavin-EM, nên dùng một viên thuốc khác. Nếu nôn xảy ra hơn 1 giờ sau khi dùng thuốc Tavin-EM, không nên dùng liều thứ hai.
Lưu ý đối với người dùng thuốc Tavin-EM
Chống chỉ định
- Chống chỉ định bệnh nhân có tiền sử quá mẫn với bất kỳ thành phần nào của thuốc
Thận trọng khi dùng
- Sự tái phân bố/tích tụ mỡ trong cơ thể, bao gồm sự béo phì phần thân và phì đại mặt trước-sau cổ (gù trâu), teo mô mỡ ở ngoại vi và mặt, phì đại tuyến vú và các biểu hiện giống hội chứng Cushing đã được báo cáo ở các bệnh nhân dùng các thuốc kháng retrovirus. Vẫn chưa rõ cơ chế và hậu quả lâu dài của các phản ứng này. Đã có các báo cáo về các trường hợp nhiễm acid lactic và gan to nhiễm mỡ nghiêm trọng, kể cả các trường hợp tử vong khi sử dụng các thuốc có cấu trúc tương tự nucleosid một mình hay kết hợp, bao gồm cả emtricitabin và tenofovir. Hội chứng phục hồi miễn dịch đã được báo cáo ở những bệnh nhân được điều trị kết hợp các thuốc kháng retrovirus.Không nên dùng thuốc này như một thành phần trong phác đồ 3 thuốc nucleosid.
Tác dụng phụ của thuốc Tavin-EM
Rất phổ biến:
- Giảm photphat huyết, đau đầu, chóng mặt, tiêu chảy, nôn mửa, buồn nôn, phát ban, tăng creatine kinase và suy nhược
Phổ biến:
- Giảm tiểu cầu, dị ứng, tăng đường huyết, tăng triglycerid huyết, mất ngủ, những giấc: mơ bất thường, tăng men transaminase, tăng amylase bao gồm tăng amylase tụy, tăng lipase huyết thanh, nôn mửa, đau bụng, khó tiêu, tăng aspartate aminotransferase huyết thanh (AST) và/ hoặc tăng alanine aminotransferase huyết thanh (ALT), tăng bilirubin máu, phát ban do viêm da niêm mạc, phát ban mụn mủ, ban đỏ, phát ban, ngứa, nổi mày đay, đổi màu da (tăng sắc tố) và đau
Không phổ biến:
- Hạ kali huyết, hạ kali do thiếu máu, globin cơ niệu kịch phát, suy cơ, tăng creatinin, protein niệu, viêm ống lượn gần bao gồm phù mạch và hội chứng Fanconi
Sử dụng thuốc ở phụ nữ có thai và cho con bú
Thời kỳ mang thai:
- Phân loại thuốc dùng trong thai kỳ: Nhóm B
- Khuyến cáo chỉ sử dụng thuốc trong quá trình mang thai nếu như thật sự cần thiết.
Thời kỳ cho con bú:
- Phụ nữ nhiễm HIV được khuyến cáo không cho con bú để tránh nguy cơ lây:truyền HIV cho trẻ sau khi sinh. Các nghiên cứu ở chuột đã chứng minh rằng tenofovir được bài tiết qua sữa mẹ. Chưa có kết luận về liệu tenofovir và emtricitabin có được bài tiết qua sữa mẹ ở người hay không. Người mẹ cần được hướng dẫn không nên cho con bú nếu đang sử dụng thuốc này do cả hai nguy cơ lây truyền HIV và xảy ra phản ứng có hại nghiêm trọng trẻ ở sơ sinh.
Ảnh hưởng đến khả năng lái xe và vận hành máy móc:
- Chưa có nghiên cứu về tác động của thuốc khi lái xe và vận hành máy móc. Tuy nhiên do một số tác dụng không mong muốn như đau đầu, chóng mặt nên cần thận trọng khi lái xe và vận hành máy móc.
Cách xử lý khi quá liều
- Trường hợp xảy ra quá liều, bệnh nhân phải được theo dõi các dấu hiệu ngộ độc và thực hiện các điều trị hỗ trợ cần thiết.
- Emtricitabin: kinh nghiệm lâm sàng còn hạn chế, hiện chỉ có ở liều cao hơn liều điều trị emtricitabin. Trong một nghiên cứu dược lý lâm sàng, liều đơn emtricitabin 1200 mg được sử dụng cho 11 bệnh nhân. Không có tác dụng không mong muốn nào được báo cáo. Trong vòng 1,5 giờ sau khi sử dụng emtricitabin, thẩm tách máu trong thời gian 3 giờ loại trừ được khoảng 30% liều emtricitabin (tốc độ dòng của máu là 400 ml/phút và tốc độ dòng của dịch thẩm tách là 600 ml/phút). Chưa có kết luận liệu emtricitabin có thể được loại bỏ bằng thẩm phân phúc mạc không.
Các biểu hiện sau khi dùng thuốc Tavin-EM
- Thông tin về biểu hiện sau khi dùng thuốc Tavin-EM đang được cập nhật.
Hướng dẫn bảo quản thuốc Tavin-EM
Điều kiện bảo quản
- Nơi khô ráo,thoáng mát, tránh ánh sáng, nhiệt độ dưới 30°C.
Thời gian bảo quản
- 24 tháng kể từ ngày sản xuất
Thông tin mua thuốc Tavin-EM
Nơi bán thuốc Tavin-EM
Nên tìm mua Tavin-EM Chợ y tế xanh hoặc các nhà thuốc uy tín để đảm bảo sức khỏe bản thân.
Giá bán
Giá sản phẩm thường xuyên thay đổi và có thể không giống nhau giữa các điểm bán. Vui lòng liên hệ hoặc đến trực tiếp điểm bán gần nhất để biết giá chính xác của thuốc vào thời điểm này.
Hình ảnh tham khảo

Nguồn tham khảo
Tham khảo thêm thông tin về thuốc Tavin-EM
Dược lực học
- Emtricitabin, chất tổng hợp tương tự nucleosid của cytosin, được phosphoryl hóa bởi enzym tế bào thanh emtricitabin 5’-triphosphat. Emtricitabin 5′-triphosphat ức chế hoạt tính của enzym sao chép ngược HIV-1 bằng cách cạnh tranh với chất nền tự nhiên deoxycytidin 5′-triphosphat và gắn vào ADN mới sinh của virus dẫn đến kết thúc chuỗi.
Dược động học
- Emtricitabin được hấp thu nhanh và nhiều sau khi uống, nồng độ đỉnh trong huyết tương (Cmax) đạt được sau 1 hoặc 2 giờ. Sinh khả dụng tuyệt đối trung bình của emtricitabin là 93% sau khi uống nhiều liều thuốc. Dưới 4% emtricitabin gắn kết với protein huyết tương. Emtricitabin không ức chế các enzym CYP450. Biến đổi sinh học xảy ra thông qua glucuronid hóa và oxy hóa. Sau khi uống emtricitabin đánh dấu 14C, 86% lượng thuốc được tìm thấy trong nước tiểu và 14% trong phân. Thời gian bán thải trong huyết tương của emtricitabin khoảng 10 giờ. Độ thanh thải ở thận của thuốc lớn hơn độ thanh thải ước tính của creatinin, cho thấy thải trừ do cả hai quá trình lọc cầu thận và bài tiết chủ động ở ống thận
Tương tác thuốc
- Sử dụng kết hợp emtricitabin với tenofovir disoproxil fumarat (TDF), zidovudin, indinavir, famciclovir và stavudin đã được nghiên cứu đánh giá ở người tình khỏe mạnh. Nồng độ đáy trong huyết tương của emtricitabin tăng 20% khi được sử dụng đồng thời với tenofovir disoproxil fumarat. Khi sử dụng đồng thời emtricitabin và zidovudin, diện tích dưới đường cong (AUC) và nồng độ đỉnh (Cmax) của zidovudin tăng tương ứng là 13% và 17%. Emtricitabin được thải trừ qua thận bằng cả hai quá trình lọc cầu thận và bài tiết chủ động ở ống thận, do đó sự cạnh tranh thải trừ có thể xảy ra với các chất khác cũng được thải trừ qua thận. Khi được sử dụng đồng thời với tenofovir disoproxil fumarat, diện tích dưới đường cong (AUC) và nồng độ đỉnh (Cmax) của didanosin dạng viên bao phim tan trong ruột và có phối hợp đệm tăng lên đáng kể. Sự tăng nồng độ didanosin với mức độ này có thể làm tăng nguy cơ xảy ra các phản ứng không mong muốn của didanosin bao gồm viêm tụy và bệnh lý thần kinh.







![[Bật mí] Phòng khám Đa khoa Việt Mỹ ở Gò Vấp có tốt không? 6 Phòng khám Đa khoa Việt Mỹ](https://songkhoe.medplus.vn/wp-content/uploads/2022/03/1590826139931.png)


![[Review] Phòng khám đa khoa Âu Á ở Hồ Chí Minh có tốt không? 9 Phòng khám đa khoa Âu Á](https://songkhoe.medplus.vn/wp-content/uploads/2022/03/phong-kham-da-khoa-o-tphcm-au-a.jpg)


![[TOP 10] bài viết về Barrett thực quản hay 2022 12 [TOP 10] bài viết về Barrett thực quản hay 2022](https://songkhoe.medplus.vn/wp-content/uploads/2022/11/TOP-10-bai-viet-ve-Barrett-thuc-quan-hay-2022.png)