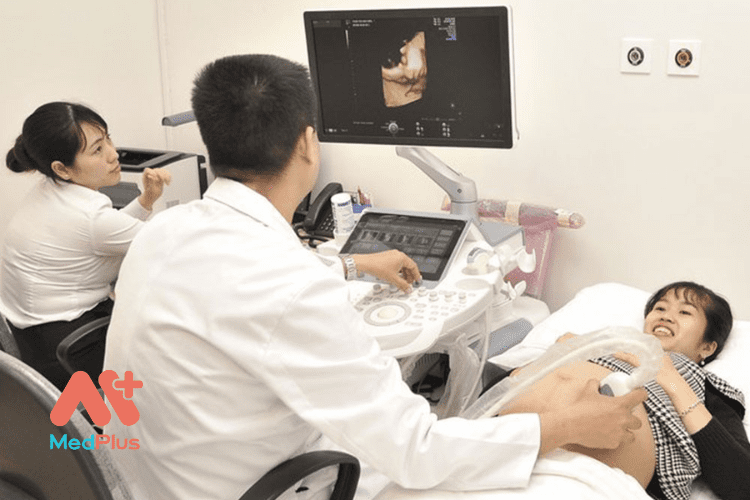
Thuốc Tevir 300 là gì?
Thuốc Tevir 300 là thuốc ETC dùng sử dụng điều trị:
- Nhiễm HIV
- Viêm gan B mãn tính
Tên biệt dược
Thuốc được đăng ký dưới tên Tevir 300
Dạng trình bày
Thuốc được bào chế dưới dạng viên nén bao phim
Quy cách đóng gói
Thuốc được đóng gói ở dạng hộp 1 chai 30 viên
Phân loại thuốc Tevir 300
Thuốc Tevir 300 là thuốc ETC– thuốc kê đơn
Số đăng ký
Thuốc có số đăng ký: VN2-99-13
Thời hạn sử dụng
Thuốc có hạn sử dụng là 24 tháng kể từ ngày sản xuất.
Nơi sản xuất
Thuốc được sản xuất ở: Ranbaxy Laboratories Ltd.
Địa chỉ: Paonta Sahib District Sirmour, Himachal Pradesh 173 025 Ấn ĐộThành phần của thuốc Tevir 300
- Tenofovir Disoproxil Fumarate (Tenofovir DF) : 300 mg tương đương Tenofovir Disoproxil : 245 mg
- Tá dược: Lactose monohydrate, Microcrystalline cellulose, Pregelatinised starch, Croscarmellose sodium, Magnesium sterate, Opadry II 31K58902 (màu trắng) và nước cất.
Công dụng của thuốc Tevir 300 trong việc điều trị bệnh
Thuốc Tevir 300 là thuốc ETC dùng sử dụng điều trị:
- Nhiễm HIV
- Viêm gan B mãn tính
Hướng dẫn sử dụng thuốc Tevir 300
Cách dùng thuốc Tevir 300
Thuốc dùng qua đường uống
Liều dùng thuốc Tevir 300
Điều trị HIV-1 hoặc viêm gan B mãn tính:
- 300 mg ngày 1 lần, không liên quan đến bữa ăn.
Liều dùng khuyến cáo ở bệnh nhi (>12 tuổi và >35 kg)
- Đối với điều trị HIV-1 ở bệnh nhi 12 tuổi trở lên có thể trọng >35 kg (>77 Ib): liều dùng là một viên nén 300 mg ngày 1 lần, bất kể liên quan đến bữa ăn.
- Hiện tại không có dữ liệu thích hợp cho bệnh nhi bị viêm gan B mãn tính.
Trẻ em và thiếu niên
- Trẻ em và thiếu niên dưới 18 tuổi không được sử dụng Bicalutamid.
Lưu ý đối với người dùng thuốc Tevir 300
Chống chỉ định
- Ở bệnh nhân trước đây đã có quá mẫn với hoạt chất hoặc với bất cứ thành phần nào của sản phẩm.
Thận trọng khi dùng thuốc Tevir 300
- Nhiễm acid lactie/ phì đại gan kèm gan nhiễm mỡ
- Đợt kịch phát viêm gan
- Nhiễm đồng thời viêm gan C hoặc D: không có dữ liệu trên hiệu lực của tenofovir ở bệnh nhân nhiễm đồng thời virus gây viêm gan C hoặc D.
- Suy chức năng thận trở nên xấu đi hoặc khởi phát mới
Tác dụng phụ của thuốc Tevir 300
- Hoại tử xương
- Tái phân bố mỡ
- Hội chứng tái lập miễn dịch
- Rối loạn chức năng ty thể
Sử dụng thuốc ở phụ nữ có thai và cho con bú
Thời kì mang thai
- Các nghiên cứu sinh sản ở chuột cống và thỏ ở các liều lên đến 14 và 19 lần liều cho người dựa trên so sánh diện tích bề mặt cơ thể cho thấy không có bằng chứng suy giảm khả năng thụ tinh hoặc gây hại cho thai nhi do tenofovir. Tuy nhiên, không có các nghiên cứu thích hợp và có đối chứng tốt ở phụ nữ có thai. Vì các nghiên cứu trên động vật không phải luôn luôn phản ánh đáp ứng ở người, nên sử dụng tenofovir trong thai kỳ chỉ khi thật cần thiết.
Thời kì cho con bú
- Khuyến cáo các bà mẹ nhiễm HIV-I không được cho con bú sữa mẹ để tránh nguy cơ truyền HIV-I sau khi sinh. Các nghiên cứu ở chuột cống chứng minh rằng tenofovir được bài tiết trong sữa. Không biết là tenofovir có bài tiết vào sữa người hay không. Vì cả khả năng truyền HIV-I và khả năng phản ứng phụ trầm trọng ở trẻ bú sữa mẹ, hướng dẫn các bà mẹ không được cho con bú bằng sữa mẹ nếu họ đang dùng tenofovir.
Ảnh hưởng đến khả năng lái xe và vận hành máy móc
Không có các nghiên cứu về tác động trên khả năng lái xe và vận hành máy móc. Tuy nhiên, bệnh nhân nên được thông báo rằng choáng váng đã được báo cáo trong khi điều trị với tenofovir disoproxil fumarate.
Cách xử lý khi quá liều
- Đã có kinh nghiệm lâm sàng hạn chế ở những liều cao hơn liều trị liệu của tenofovir DF 300mg. Trong nghiên cứu IV, 600 mg tenofovir DF được dùng cho 8 bệnh nhân uống trong 28 ngày. Không có phản ứng phụ trầm trọng nào đã được báo cáo. Không biết các tác động của các liều cao hơn.
- Nếu xảy ra quá liều, bệnh nhân phải được giám sát về bằng chứng về ngộ độc, và điều trị hỗ trợ khi cần thiết.
- Tenofovir được đào thải hiệu quả bằng thẩm phân máu với hệ số lọc máu xấp xỉ 4%. Sau liều đơn 300mg tenofovir DF, một đợt thẩm phân máu kéo dài 4 giờ loại bỏ khoảng 10% liều dùng tenofovir đã được dùng.
Các biểu hiện sau khi dùng thuốc Tevir 300
- Thông tin về biểu hiện sau khi dùng thuốc Tevir 300 đang được cập nhật.
Hướng dẫn bảo quản thuốc Tevir 300
Điều kiện bảo quản
- Nơi khô ráo,thoáng mát, tránh ánh sáng, nhiệt độ dưới 30°C.
Thời gian bảo quản
- 24 tháng kể từ ngày sản xuất.
Thông tin mua thuốc Tevir 300
Nơi bán thuốc Tevir 300
Nên tìm mua thuốc Tevir 300 Chợ y tế xanh hoặc các nhà thuốc uy tín để đảm bảo sức khỏe bản thân.
Giá bán
Giá sản phẩm thường xuyên thay đổi và có thể không giống nhau giữa các điểm bán. Vui lòng liên hệ hoặc đến trực tiếp điểm bán gần nhất để biết giá chính xác của thuốc vào thời điểm này.
Hình ảnh tham khảo

Nguồn tham khảo
Tham khảo thêm thông tin về thuốc Tevir 300
Đặc tính dược lực học:
Hoạt tính kháng virus:
- Hoạt tính kháng virus của tenofovir trong xét nghiệm cận lâm sàng và ở các chủng phân lập của HIV-I đã được đánh giá ở các dòng nguyên bào lympho, các tế bào đơn nhân nguyên thủy/đại thực bào và các tế bào lympho trong máu ngoại biên.
Đề kháng:
- Các chủng đề kháng HIV-1 giảm độ nhạy cảm với tenofovir đã được chọn lọc ở tế bào nuôi cấy. Các virus này có một góc thế K65R 6 men phiên mã ngược và cho thấy giảm độ nhạy cảm với tenofovir 2- 4 lần.
Đề kháng chéo:
- Đề kháng chéo giữa một số chất ức chế men phiên mã ngược nào đó đã được phát hiện. Gốc thế K65R được chọn lọc bởi tenofovir cũng được chọn lọc ở một số bệnh nhân nhiễm HIV-1 được điều trị với abacavir, didanosine, hoặc zalcitabine. Các chủng phân lập HIV-1 với đột biến này cho thấy cũng bị giảm độ nhạy cảm với emtricitabine và lamivudine. Vì vậy, đề kháng chéo giữa các thuốc này có thể xảy ra ở bệnh nhân có virus gốc thế K65R ẩn náu. Các chủng phân lập từ bệnh nhân có HIV-I biểu lộ trung bình 3 gốc thế men phiên mã ngược liên quan với zidovudine (M41L, D67N, K70R, L210W, T215Y/F, hoặc K219Q/E/N), cho thấy giảm nhạy cảm với tenofovir 3,1 lan. HIV-1 dé khang da nucleoside có một gốc thế chèn gấp đôi T69S trong men phiên mã ngược cho thấy giảm nhạy cảm với tenofovir.
Đặc tính dược động học:
- Về thực chất những nồng độ cao hơn (-300 lần) nồng độ quan sát được in vitro, tenofovir không ức chế chuyển hóa thuốc trên in vitro qua trung gian bởi bất kỳ trong số các isoform CYP 6 người: CYP3A4, CYP2D6, CYP2C9, hoặc CYP2E1. Tuy nhiên, một lượng nhỏ (6%) nhưng giảm đáng kể có ý nghĩa thống kê về chuyển hóa của cơ chất CYPIA da được quan sát. Dựa vào các kết quả của các thí nghiệm in vitro và đường đào thải đã được biết của tenofovir, khả năng cho các tương tác qua trung gian CYP gồm tenofovir với các thuốc khác là thấp
Tương tác thuốc
Sử dụng đồng thời không được khuyến cáo:
- Không dùng tenofovir với bất kỳ thuốc nào chứa tenofovir disoproxil fumarate.
- Không dùng tenofovir đồng thời với adefovir dipivoxil.
Didanosine:
- Không khuyến cáo sử dụng đồng thời tenofovir disoproxil fumarate và didanosine
Các thuốc được đào thải qua thận:
- Vì tenofovir được đào thải chủ yếu bởi thận, sử dụng đồng thời tenofovir disoproxil fumarate với các thuốc làm giảm chức năng thận hoặc cạnh tranh trên sự tiết chủ động qua ống thận thông qua protein vận chuyển hOAT 1, hOAT 3 hoặc MRP4 (như cidofovir) có thể làm tăng nồng độ huyết thanh của tenofovir và/hoặc các thuốc dùng đồng thời.
- Nên tránh sử dụng đồng thời hoặc gần đây có sử dụng thuốc gây độc thận kèm với tenofovir disoproxil fumarate. Một số ví dụ gồm, nhưng không có giới hạn, aminoglycosides, amphotericin B, foscarnet, ganciclovir, pentamidine, vancomycin, cidofovir hoặc interleukin – 2







![[Bật mí] Phòng khám Đa khoa Việt Mỹ ở Gò Vấp có tốt không? 6 Phòng khám Đa khoa Việt Mỹ](https://songkhoe.medplus.vn/wp-content/uploads/2022/03/1590826139931.png)


![[Review] Phòng khám đa khoa Âu Á ở Hồ Chí Minh có tốt không? 9 Phòng khám đa khoa Âu Á](https://songkhoe.medplus.vn/wp-content/uploads/2022/03/phong-kham-da-khoa-o-tphcm-au-a.jpg)


![[TOP 10] bài viết về Barrett thực quản hay 2022 12 [TOP 10] bài viết về Barrett thực quản hay 2022](https://songkhoe.medplus.vn/wp-content/uploads/2022/11/TOP-10-bai-viet-ve-Barrett-thuc-quan-hay-2022.png)